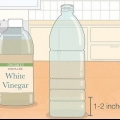
Puedes seguir recolectando el gas mientras ocurra la reacción. Para demostraciones en el aula, solo necesita una pequeña cantidad de ácido clorhídrico, que se diluye a 1 M; una concentración de 2 M funciona mejor, pero debe usarse con mucho cuidado ya que es un ácido fuerte. La ecuación es: CaCO3(s) + 2HCl(aq) ==> CaCl2(ac) + H2O(l) + CO2(gramo). Tenga mucho cuidado cuando trabaje con ácido clorhídrico: use guantes, una bata de laboratorio y gafas protectoras, y no permita que el ácido entre en contacto con su piel! Es mejor realizar esta reacción solo en un entorno de laboratorio. 


Coloque 1 cucharadita de hidróxido de calcio en una botella de vidrio limpia de 4 litros o menos. El agua de cal es una solución saturada, lo que significa que habrá un químico adicional que no se disolverá. Una cucharadita dará como resultado una solución completamente saturada, ya sea que tome una botella de 4 litros o una más pequeña. Llene la botella con agua destilada. Lo mejor es usar agua destilada para este experimento, ya que le dará una solución más pura. Cierra la botella con una tapa. Agite la solución vigorosamente durante 1-2 minutos y luego déjela reposar durante 24 horas. Vierta la solución purificada desde la parte superior del frasco a través de un filtro de café limpio o papel de filtro. Tenga cuidado de no revolver el sedimento. Si es necesario, repita este filtrado hasta obtener una solución clara de cal. Guárdelo en un frasco o botella limpios. 
Si no quieres hervirlo, también puedes usar una jeringa de gas para eliminar el CO2 directamente en el tubo de ensayo de agua con cal medio lleno. Tape el tubo de ensayo y luego agítelo vigorosamente durante 1-2 minutos. Si hay dióxido de carbono en la muestra, la solución debe volverse turbia. 

Si tienes el CO2 a través del agua de cal durante un período de tiempo más largo, el agua eventualmente se volverá clara. Esto se debe a una reacción química! Aquí está esta respuesta: CO2 + eh2==> eh2CO3 (dióxido de carbono + agua = dióxido de carbono) eh2CO3 + CaCO3 ==> Ca(HCO3)2(ácido carbónico + carbonato de calcio = hidrogenocarbonato de calcio) El hidrogenocarbonato de calcio es soluble en agua, lo que hace que su solución sea transparente! 



Probar si un gas es dióxido de carbono
Contenido
Dióxido de carbono (CO2) es incoloro e inodoro, por lo que no se puede detectar por observación directa. Necesita recolectar una muestra de aire (o un CO2 muestra) y luego realice una de muchas pruebas simples para determinar la presencia del gas. Puede hacer pasar el gas a través de agua calcárea, o puede sostener una astilla de madera incandescente en el gas para ver si la presencia de CO2 se extingue.
Pasos
Método 1 de 3: preparar una muestra

1. Recoge un CO2 muestra. Para comenzar su prueba, necesitará un tubo de ensayo sellado lleno de gas recolectado. Puede capturar dióxido de carbono en una botella de gas, un tubo de ensayo calentable u otro recipiente hermético. La recolección generalmente se realiza sobre el agua en una taza medidora. CO2 el gas es más denso que el aire, por lo que puede atraparlo usando `entrega hacia abajo` o una jeringa.

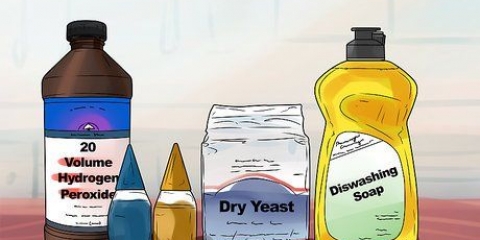
2. Mezclar carbonato de calcio con ácido clorhídrico (HCl). La forma más fácil de capturar dióxido de carbono es haciendo reaccionar carbonato de calcio (o virutas de cal) con ácido clorhídrico. Primero vierta 20 ml de HCl en un matraz Erlenmeyer. Agregue una cucharada de carbonato de calcio (o virutas de piedra caliza) al HCL. Cuando comience la reacción, cubra el matraz Erlenmeyer con un corcho y una tubería: recolecte el gas a través de la tubería y en un tubo de ensayo invertido (que está sumergido en un recipiente con agua). Si el nivel del agua en el tubo de ensayo cambia, el gas se recolecta.

3. Cierra el tubo de ensayo con un corcho (el `tapón`). Por seguridad, coloque el tubo de ensayo en una rejilla hasta que vaya a realizar la prueba. El `tapón` es esencialmente un pequeño corcho o tapa que le permite dirigir el contenido del tubo de ensayo a otro lugar a través de una tubería conectada. Es importante reducir el CO2 cerrar el gas en el contenedor. Si lo deja abierto, el gas se mezclará con el aire y su prueba será mucho menos efectiva.
Método 2 de 3: pasa el gas por agua con cal

1. Pasar el gas por el agua de cal. La forma más efectiva de hacer la prueba de CO2 es pasando el gas a través de `agua de cal` (una solución diluida de hidróxido de calcio (cal apagada)). Cuando burbujeas dióxido de carbono a través de la solución, forma un precipitado sólido de carbonato de calcio y piedra caliza. El carbonato de calcio es insoluble en agua. Entonces, si hay CO2 presentes en la muestra, el agua de cal se volverá lechosa y turbia.
- El agua de cal también se llama `lavado blanco` o `lechada de cal`. Cuando vea estos términos, sabrá que se trata de agua con cal.

2. Hacer una solución de cal. El proceso es simple: diluir hidróxido de calcio con agua. Hidróxido de calcio (Ca(OH))2) es un polvo blanco incoloro que puedes comprar en la mayoría de las farmacias. El agua de cal pura, una vez mezclada, es transparente e incolora, con un ligero olor a tierra y el sabor amargo y alcalino del hidróxido de calcio, ya que su valor de pH es de 12,3. Sigue estos pasos para hacer tu propia agua de cal:

3. Pasar el gas por el agua de cal. Llene un tubo de ensayo hasta la mitad con agua de cal y luego hiérvalo. Utilice una tubería para medir el contenido de CO2 tubo de ensayo de prueba directamente en el agua de cal hirviendo. Puede usar un tubo flexible o una pajita (metálica) como tubería, si no hay nada mejor alrededor. Deje que el gas recogido "burbujee" a través del líquido y espere a que se produzca la reacción.

4. Cuidado con el agua turbia. Si CO2 presentes, el agua de cal se volverá de color blanco lechoso debido a las partículas de carbonato de calcio, ya que la solución de carbonato de calcio es insoluble y se precipitará fuera de la solución. Si el agua de cal está hirviendo y el gas se introduce directamente en el agua de cal, la reacción debe comenzar de inmediato. Si no sucede nada después de aproximadamente un minuto, entonces puede asumir con seguridad que no hay dióxido de carbono en su muestra.

5. Aprende la reacción química. Comprenda qué sucede exactamente para detectar la presencia de CO2 indicar. La ecuación para la prueba es: Ca(OH)2 (ac) + CO2 (g) ==> CaCO3 (s) + H2O (l). En lenguaje sencillo: agua de cal líquida + gas (que CO2 contiene) reacciona con la cal (las partículas) y el agua.
Método 3 de 3: prueba con una viruta de madera brillante

1. Comprobar si el gas extingue el fuego. Dióxido de carbono en altas concentraciones, extingue incendios. Todo lo que necesita hacer es sostener una pequeña llama encendida en un tubo de ensayo que sospeche que contiene CO2 contiene. Si el gas está presente, la llama debe extinguirse inmediatamente. La ignición (crear una llama) es la reacción del oxígeno con otra sustancia; es una oxidación rápida del compuesto orgánico y una disminución del oxígeno. El fuego se apaga porque el oxígeno es reemplazado por el CO2, que no es un gas combustible.
- Tenga en cuenta que cualquier gas libre de oxígeno también extinguirá una llama de esta manera. Por lo tanto, esta es una prueba poco confiable para el dióxido de carbono y puede conducir a una identificación errónea del gas.

2. Recoja el gas en un tubo de ensayo invertido. Asegúrese de que la muestra esté correctamente almacenada y sellada antes de intentar realizar la prueba de CO2. Esté razonablemente seguro de que el tubo de ensayo no contiene gases inflamables o explosivos, en cuyo caso el fuego como prueba puede ser peligroso o, al menos, muy aterrador.

3. Coloque una pequeña llama en el tubo de ensayo. Use una paleta o una tira de madera larga y delgada. Un fósforo o un encendedor también serán suficientes, pero cuanto más lejos estén sus manos de la abertura del tubo de ensayo, más seguro será su experimento. Si la llama se apaga inmediatamente, probablemente haya una alta concentración de CO2 presente en el tubo de ensayo.

4. Alternativamente, también puede usar una jeringa de gas para apagar una vela. Llene una jeringa con dióxido de carbono. Luego use una gota de cera derretida para aplicar una vela corta a la superficie de una moneda. Luego coloque la vela y la moneda en una taza ancha y encienda la vela. Coloque el tubo en la jeringa e inyecte el CO2 al fondo de la copa. Si saca todo el contenido de la jeringa en uno o dos segundos, la llama debería apagarse.
Artículos de primera necesidad
- Agua de lima
- Tubo de ensayo resistente al calor
- jeringa de gas
- Tubo (tubo de suministro)
- CO2 muestra (o solo agua)
Artículos sobre el tema. "Probar si un gas es dióxido de carbono"
Оцените, пожалуйста статью
Popular