Tenga cuidado con las cubetas, ya que pueden ser bastante caras, especialmente si son de vidrio o cuarzo. Las cubetas de cuarzo están diseñadas para su uso en espectrofotometría UV-visible. Al manipular la cubeta, no toque los lados por los que pasará la luz (generalmente, los lados transparentes del tubo). Si toca accidentalmente estos lados, limpie la cubeta con un `kimwipe` (que están formulados para evitar rayar el vidrio). 
Si usa una pipeta para cargar sus muestras, use una punta nueva para cada muestra para evitar la contaminación cruzada. 



Los espectrofotómetros digitales se pueden calibrar de la misma manera, solo tendrán una lectura digital. Establezca el blanco a cero con las perillas de ajuste. Cuando quita el blanco, la calibración sigue siendo correcta. Al medir el resto de las muestras, automáticamente se resta la absorbancia del blanco. Asegúrese de usar un solo blanco por sesión para que cada muestra se calibre con el mismo blanco. Por ejemplo, si vacía el espectrofotómetro, luego analiza solo unas pocas muestras y vuelve a vaciar el espectrofotómetro, las muestras restantes serán inexactas. Entonces tienes que empezar de nuevo. 
Si la aguja o la lectura no es cero, repita los pasos de calibración con el blanco. Si continúa teniendo problemas, obtenga ayuda o haga que revisen el dispositivo para detectar problemas. 
La absorbancia también se conoce como la densidad óptica (OD). Cuanta más luz se deja pasar, menos luz absorbe la muestra. En general, anotará los valores de absorbancia, que generalmente se darán como decimales. Por ejemplo: 0,43. Si obtiene un resultado anormal (como 0,900 mientras que el resto está alrededor de 0,400), diluya la muestra y mida la absorbancia nuevamente. Repita la medición para cada muestra individual al menos tres veces y promedie las mediciones. Esto proporciona una lectura más precisa. 


Un espectro de absorción generalmente tiene picos en ciertas longitudes de onda que le permiten identificar compuestos específicos. 
También puede usar este método para identificar contaminantes en su muestra. Si espera un pico claro en una cierta longitud de onda y obtiene dos picos en diferentes longitudes de onda, entonces sabe que algo anda mal en su muestra.
Realizar un análisis espectrofotométrico
Contenido
La espectrofotometría es una técnica experimental utilizada para medir la concentración de solutos en una solución específica, calculando la cantidad de luz absorbida por esos solutos. Esta técnica es poderosa porque ciertos compuestos absorberán diferentes longitudes de onda de luz con diferentes intensidades. Al analizar la luz que pasa a través de la solución, puede identificar ciertos solutos en la solución y qué tan concentradas están esas sustancias. Un espectrofotómetro es el dispositivo utilizado para analizar soluciones en un entorno de laboratorio.
Pasos
Parte 1 de 3: preparación de las muestras

1. Enciende el espectrofotómetro. La mayoría de los espectrofotómetros necesitan calentarse antes de que puedan dar una lectura precisa. Encienda el dispositivo y déjelo reposar durante al menos 15 minutos antes de analizar las muestras.
- Utilice el tiempo de calentamiento para preparar sus muestras.

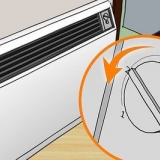
2. Limpiar las cubetas o tubos de ensayo. Si está haciendo un laboratorio escolar, es posible que esté usando tubos de ensayo desechables que no necesitan limpiarse. Si utiliza cubetas o tubos de ensayo reutilizables, asegúrese de limpiarlos bien antes de usarlos. Enjuague bien cada cubeta con agua desionizada.

3. Cargue el volumen apropiado de muestra en la cubeta. Algunas cubetas tienen un volumen máximo de 1 mililitro (ml), mientras que los tubos de ensayo pueden tener un volumen máximo de 5 ml. Siempre que el láser que produce la luz atraviese el líquido y no una parte vacía del recipiente, obtendrá una lectura precisa.

4. Hacer una solución de control. La solución de control, o `blanco`, tiene solo el solvente químico en el que se disuelve la solución a analizar. Por ejemplo, si disolvió sal en agua, su `blanco` contendría solo agua. Si colorea el agua de rojo, el espacio en blanco también debe contener agua roja. El blanco tiene el mismo volumen que la solución a analizar y se mantiene en el mismo tipo de recipiente.

5. Limpie el exterior de la cubeta. Antes de colocar la cubeta en el espectrofotómetro, debe asegurarse de que esté lo más limpia posible para evitar la interferencia de suciedad o partículas de polvo. Utilice un paño sin pelusa para eliminar las gotas de agua o el polvo que pueda haber en el exterior de la cubeta.
Parte 2 de 3: ejecutar el experimento

1. Elija y configure la longitud de onda de la luz para analizar la muestra con. Use una sola longitud de onda de luz (color monocromático) para que la prueba sea más efectiva. El color de la luz debe ser un color que se sepa que es absorbido por una de las sustancias químicas que se sospecha que están presentes en la solución de prueba. Configure la longitud de onda deseada de acuerdo con las especificaciones de su espectrofotómetro.
- En el laboratorio de un salón de clases, la longitud de onda probablemente se dará.
- Dado que la muestra reflejará toda la luz del mismo color cuando aparezca, la longitud de onda experimental siempre será de un color diferente al de la muestra.
- Los objetos aparecen en ciertos colores porque reflejan la luz de ciertas longitudes de onda y absorben todos los demás colores. El pasto es verde porque la clorofila en el pasto refleja la luz verde y absorbe todo lo demás.

2. Calibre la máquina con el `blanco`. Coloque el blanco en el portacubetas y cierre la tapa. En un espectrofotómetro analógico habrá una pantalla con una aguja que se mueve según la intensidad de la detección de luz. Cuando el espacio en blanco está adentro, debería ver que la aguja se mueve hacia la derecha. Tenga en cuenta este valor en caso de que lo necesite más tarde. Con el blanco todavía en la máquina, ajuste la aguja a cero con la perilla de ajuste.

3. Retire el blanco y pruebe la calibración. Con el espacio en blanco retirado, la aguja debe permanecer en 0 (cero) o la lectura digital debe permanecer en cero. Vuelva a colocar el blanco en el dispositivo y verifique que la aguja o la lectura no cambien. Si la máquina está correctamente calibrada con su blanco, todo debería quedar en cero.

4. Mida la absorbancia de su muestra experimental. Retire el blanco y coloque la muestra experimental en el dispositivo. Deslice la cubeta en la ranura adecuada y asegúrese de que esté en posición vertical. Espere unos 10 segundos para que la aguja se detenga o para que los números digitales dejen de cambiar. Anotar los valores de % de transmisión y/o absorbancia.

5. Repita la prueba con sucesivas longitudes de onda de luz. Su muestra puede contener múltiples compuestos desconocidos cuya absorbancia varía según la longitud de onda. Para descartar la incertidumbre, repita las mediciones a intervalos de 25 nm en todo el espectro. De esta manera, puede detectar otras sustancias químicas que sospecha que están en el soluto.
Parte 3 de 3: análisis de los datos de absorbancia

1. Calcular la transmisión y la absorbancia de la muestra. La transmisión indica la cantidad de luz que pasó a través de la muestra que llegó al espectrofotómetro. La absorción es la cantidad de luz que ha sido absorbida por una de las sustancias químicas del soluto. Muchos espectrofotómetros modernos muestran transmisión y absorción, pero una vez que haya registrado la intensidad, puede calcular estos valores.
- La transmitancia (T) se encuentra dividiendo la intensidad de la luz que ha pasado a través de la solución de muestra por la cantidad que ha pasado a través del blanco. Suele expresarse como decimal o como porcentaje. T = yo/yo0 donde I es la intensidad de la muestra y I0 la intensidad del blanco.
- La absorbancia (A) se expresa como el negativo del logaritmo (exponente) del valor de transmisión (base-10): A = -log10t. Para un valor T de 0,1, el valor de A es 1 (0,1 es 10 a la -1ª potencia), lo que significa que el 10 % de la luz se transmite y el 90 % se absorbe. Para un valor T de 0,01, el valor de A es 2 (0,01 es 10 a la -2ª potencia), lo que significa que se transmite el 1 % de la luz.

2. Trace los valores de absorbancia contra las longitudes de onda en un gráfico. El valor de absorbancia se traza en el eje vertical y contra la longitud de onda de la luz utilizada para una prueba particular trazada en el eje horizontal x. Trazar los valores máximos de absorbancia para cada longitud de onda de la luz analizada produce el espectro de absorbancia de la muestra e identifica los compuestos que componen el químico de prueba y sus proporciones.

3. Compare su gráfico de espectro de absorción con gráficos conocidos de compuestos específicos. Los compuestos tienen un espectro de absorción único y siempre producirán un pico en la misma longitud de onda cada vez que se miden. Al comparar sus gráficos de compuestos desconocidos con los de compuestos conocidos, puede identificar los solventes que componen su solución.
Artículos de primera necesidad
- Espectrofotómetro
- Sustancia en la solución a analizar
- Extra solvente o solvente (para una solución en blanco)
- Recipientes para soluciones de prueba y en blanco (cubetas, tubos de ensayo, etc.).)
Artículos sobre el tema. "Realizar un análisis espectrofotométrico"
Оцените, пожалуйста статью
Popular